|
癌症免疫疗法是日前正在科研的新办法之一,旨在为癌症病人发掘更好的结果的新机会,其中包含树突状细胞(DC)疫苗疗法。
关于DC细胞
美国专家拉尔夫斯坦曼于1973年发掘DC细胞,树突状细胞(DC)是一类存在于血液、组织和淋巴器官中的骨髓源自细胞。从广义上讲,DC的功能是桥接先天免疫系统和适应性免疫系统,是免疫系统的“哨兵”。在面对外敌入侵时,尤其是癌细胞时,DC细胞在全部免疫过程能够调动其他的肿瘤杀伤细胞,是身体功能最强的抗原提呈细胞。DC细胞做为抗原递送载体是癌症疫苗的重点焦点,科研人员经过数十年的奋斗,最终“物尽其用”开发出针对各类癌种的树突细胞疫苗。
2007年斯坦曼确诊了胰腺癌,晚期胰腺癌患者一般预后较差。之后便积极尝试基于树突状细胞的治疗性疫苗(DC疫苗),并借助DC疫苗将预期数月的生命延长至四年半。2011年,斯坦曼因发掘DC而得到诺贝尔奖。
日前,都数树突细胞疫苗已然被国际医学抗肿瘤行业广泛认可,并已然应用于多种癌症的临床治疗中,这是癌症病人治疗的期盼。
首个针对癌症的治疗性DC疫苗-Sipuleucel-T疫苗
2010年,美国FDA准许了Sipuleucel-T疫苗,这是一种针对晚期转移性前列腺癌的疫苗,亦是第1种针对癌症的治疗性DC疫苗,将癌症免疫治疗带入了一个新时代。
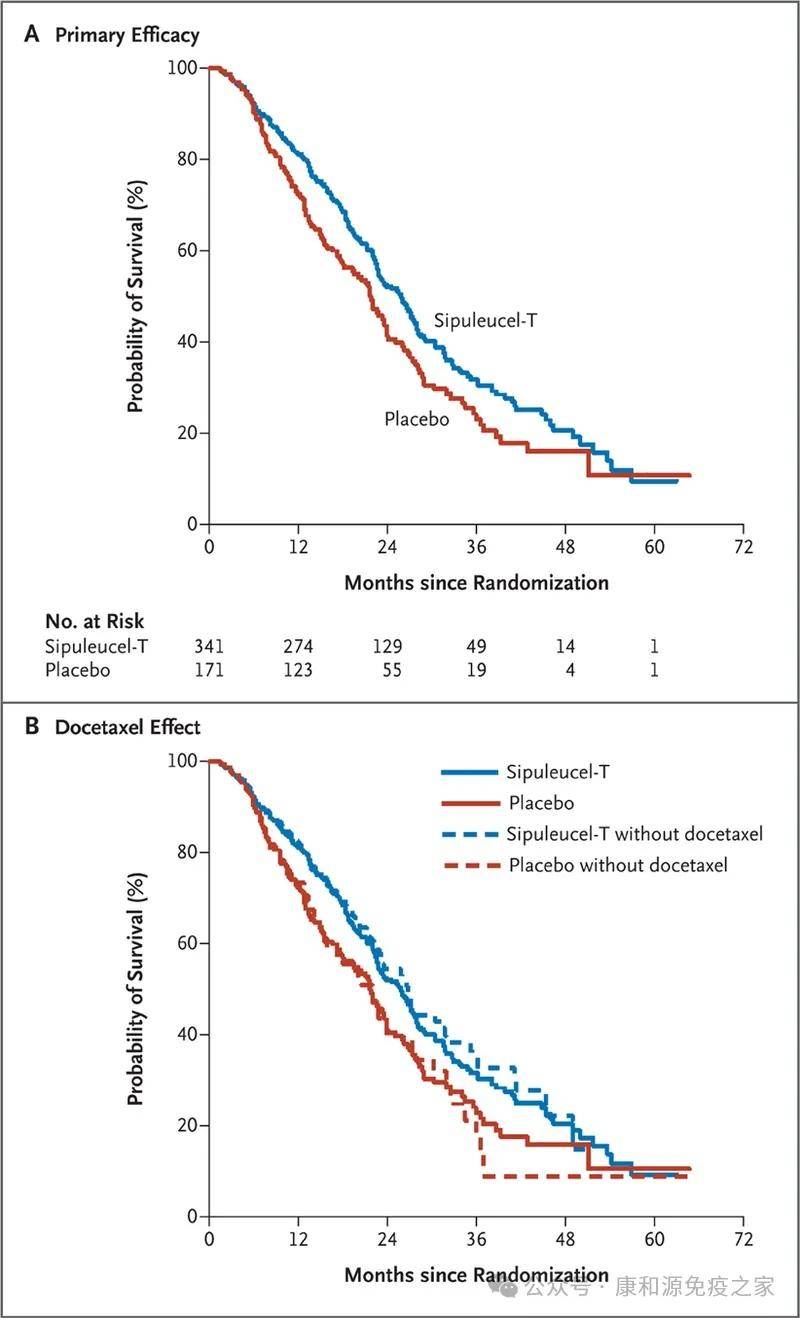
一项双盲、安慰剂对照、多中心实验,触及512名身患转移性前列腺癌的男性,其中 341 名病人接受 sipuleucel-T,171 名病人接受安慰剂治疗。科研结果表示,与安慰剂组相比,sipuleucel-T组的死亡危害相对降低22%,这一减少显示中位存活期加强了4.1个月(sipuleucel-T组为25.8个月,安慰剂组为21.7个月)。sipuleucel-T组36个月存活率为31.7%,安慰剂组为23.0%。
没发展存活期超577天!WT1脉冲树突状细胞疫苗为终末期肺癌病人带来曙光
WT1是一种平常的癌症抗原,在多种肿瘤中广泛表达,既可用于治疗血液肿瘤,亦可用于治疗肺癌、胃癌、肝癌、乳腺癌等多款实体瘤。WT1脉冲树突状细胞(WT1-DC)疫苗是一种抗癌免疫细胞疗法,运用病人自己的单核细胞进行体外培养和分化。据报告,WT1-DC在晚期癌症中是成功的。
2023年10月,著名医学杂志《Cureus》发布了一篇“采用WT1-DC联合二线化疗治疗改善终末期肺癌的免疫特征并延长没发展存活期”。
该病人为被诊断为右肺中叶 IV 期鳞状细胞癌并伴有双侧肾上腺转移、多发性肝转移和多发性骨转移的69 岁男性。此时该病人已没法耐受手术和放疗。
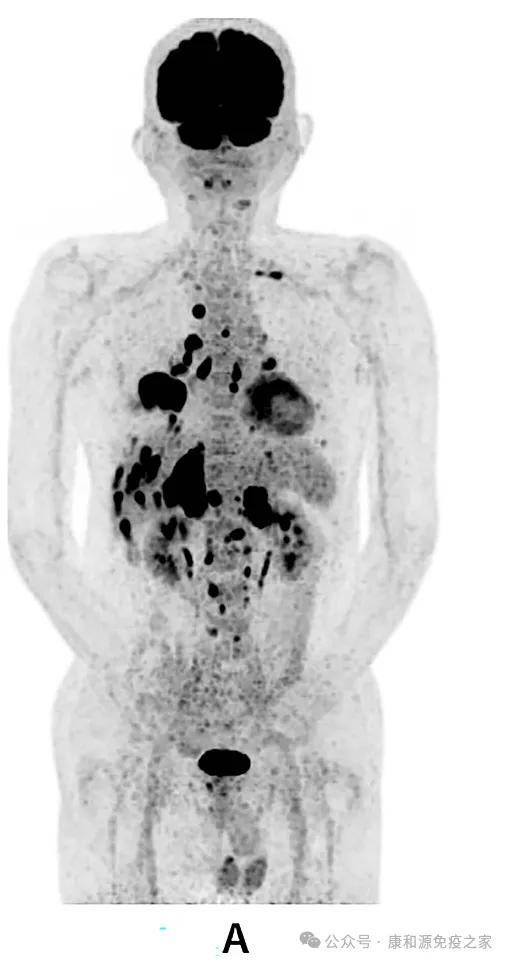
给予卡铂 (CBDCA) AUC6 和紫杉醇(PTX)每三周给药一次,连续四个周期(直到第1次诊断后第84天)。结果,与治疗起始时(第0天)的胸部CT相比,第114天的胸部CT观察到癌症显著缩小。诊断时的癌胚抗原(CEA)为 66.4,但在第121天降至3.0。然而,第121天的N/L比值高达5.18,中性粒细胞比值高(79.2%),淋巴细胞比值低(15.3%)。直到第155天,这里时期CEA增多到3.6。

病人从第 155 天起始每两周起始一次 WT1-DC。从病人外周血中收集的单核细胞在细胞培养实验室中分化为成熟的树突状细胞。在树突状细胞培养过程中,用WT1抗原脉冲它们进行抗原识别。将成熟的树突状细胞分别皮下注射到左腹股沟淋巴结和右腹股沟淋巴结周边。直到第280天共接种了8剂。
第479天的PET-CT表示,除了右肺2个直径1.0cm的转移性病灶和肝脏1个直径1.7cm的转移性病灶外,无反常发掘。截止数据统计时,该病人没发展存活期(PFS)已超577天,病人临床情况良好,能够正常的平常生活。
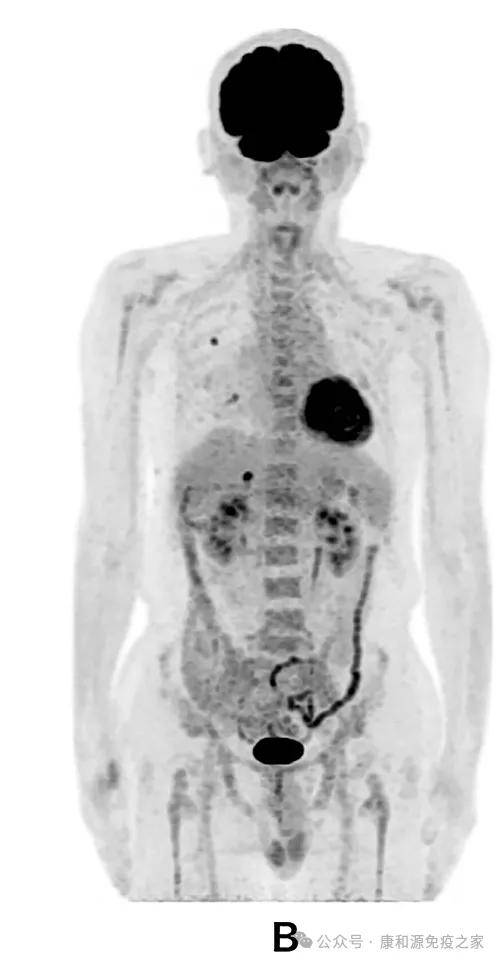
结果显示,WT1-DC改善了病人免疫系统,并可长时间维持化疗的明显效果。
DC疫苗联合过继性T细胞辅助治疗肝癌,71.4%病人没复发!
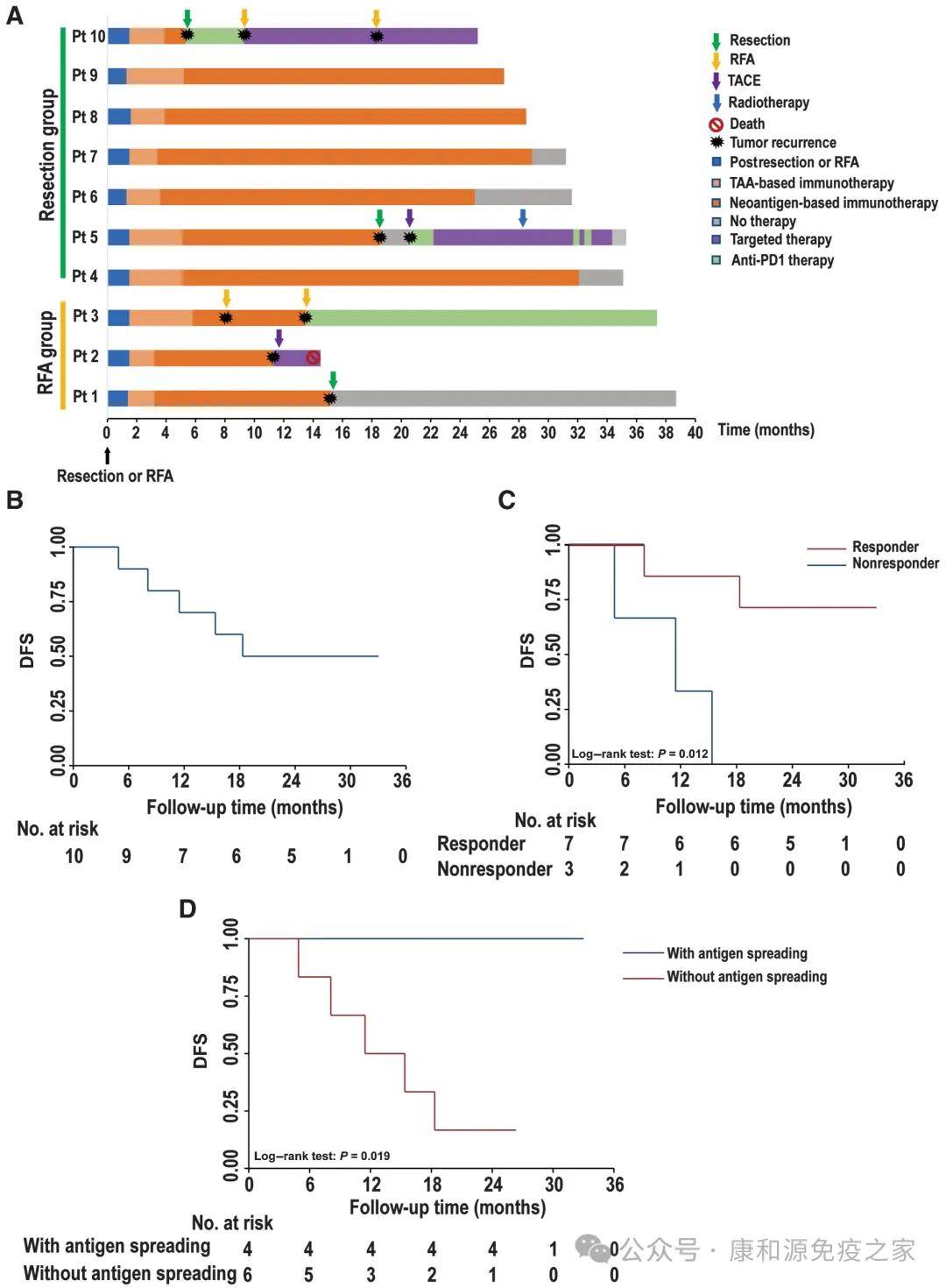
2022年6月,中国科研团队在美国癌症科研协会(AACR)旗下要紧期刊《Cancer Immunology Research》发布了一项DC疫苗联合过继性T细胞辅助治疗肝癌的科研论文,报告了REMEC临床实验(NCT03067493)第1周期的前期结果。该临床实验是全世界首个基于肿瘤新生抗原的树突状细胞(DC)疫苗和过继性T细胞联合疗法预防肝癌复发的Ⅱ期临床实验。
从2017年9月25日到2018年11月26日,10例病人接受了辅助联合免疫治疗,5例病人在根治性治疗后2年内未复发,中位没疾患存活期(DFS)为18.3个月。其中71.4%的免疫应答者在根治性治疗后2年内未复发。
黑色素瘤—TLPLDC疫苗
DC疫苗与免疫检测点控制剂(ICIs)的组合,已被证明可治疗黑色素瘤。TLPLDC(肿瘤裂解物、颗粒负载、树突状细胞)疫苗是一种独特的免疫疗法,可将病人的完整肿瘤抗原库传递给免疫系统,产生双重先天性和适应性免疫反应,激活战斗机T细胞,并触发免疫系统识别、寻找并摧毁任何含有该抗原的细胞,达到治疗目的。
一项随机、双盲、安慰剂对照 2b 期实验表示TLPLDC疫苗治疗黑色素瘤可加强临床疗效。随机分配了 144 名病人。疫苗组共有 103 例病人,对照组 41 例。结果表示:在中位随访27.0个月时,疫苗组的 36 个月估计没疾患存活期(DFS)为 38.1%,安慰剂组为 30.0%。疫苗组的 36 个月估计总存活期(OS)为 80.1%,安慰剂组为 70.9%。
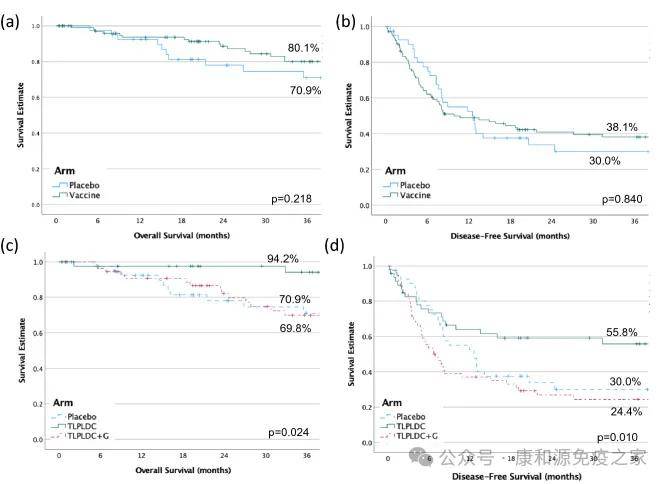
由此可见DC疫苗在各大癌种中均取得了不俗的疗效。
怎样参加DC疫苗的临床科研
MASCT-I是由于恒瑞源正开发的细胞治疗制品,其活性成分包含负载多种肿瘤关联抗原的成熟自体树突状细胞(简叫作“DC细胞”)和DC细胞活化扩增的自体效应T淋巴细胞(简叫作“T细胞”),经过二者序贯治疗清除肿瘤。MASCT-I于2018年在中国获准单药治疗恶性实体瘤的临床科研。在纳入的10例一线化疗后获益的尿路上皮癌病人中,有1例显现部分缓解,60%以上的病人均达到病情稳定。
好信息是,MASCT-I日前在国内多中心开展临床实验,日前正在招募病人,想申请的病友能够联系康和源免疫之家医学部(400-880-3716)认识仔细的出入排标准,并进行初步评定,看是不是有机会申请临床实验。
项目名叫作:MASCT-I用于晚期尿路上皮癌受试者标准一线化疗获益后维持治疗的II期临床科研
部分入排标准:
1.预计存活期≥6个月;
2.ECOG评分为0或1分;
3.晚期一线化疗前拥有可评定病灶;
4.化疗完成后的疗效评定为CR、PR或SD(包含一线化疗前仅有非靶病灶,化疗完成后疗效评定为非CR非PD者)的尿路上皮癌(尿路上皮癌包含肾癌、尿道癌、膀胱癌以及输尿管癌)。
想要寻求临床实验帮忙的病人可提交病理报告、治疗经历等资料至康和源免疫之家医学部(400-880-3716)进行初步评定。
综上所述,DC疫苗是一种拥有广阔应用前景的新兴免疫治疗办法。DC做为抗原提呈细胞,可激活T细胞并诱导效应抗肿瘤反应,在机体免疫过程中发挥着要紧功效。相信随着免疫疗法的发展,DC疫苗将会在癌症治疗方面发挥要紧功效,将为更加多癌症病人带来治疗期盼。
参考资料
Original research: Prospective, randomized, double-blind phase 2B trial of the TLPO and TLPLDC vaccines to prevent recurrence of resected stage III/IV melanoma: a prespecified 36-month analysis - PMC (nih.gov)
免责声明:康和源免疫之家为免疫科普平台,文本参考源自于网络,版权归原作者所有。
该文案仅供分享,如涉嫌侵犯您的著作权请联系咱们删除,谢谢!返回外链论坛:http://www.fok120.com/,查看更加多
责任编辑:网友投稿
|